Die Korrosionsrate ist ein multifaktorieller Parameter, der sowohl von den äußeren Umgebungsbedingungen als auch von den inneren Eigenschaften des Materials abhängt. In der normativen und technischen Dokumentation gibt es bestimmte Einschränkungen der zulässigen Werte der Metallzerstörung während des Betriebs von Geräten und Gebäudestrukturen, um deren störungsfreien Betrieb zu gewährleisten. In der Technik gibt es keine universelle Methode zur Bestimmung der Korrosionsrate. Dies liegt an der Komplexität der Berücksichtigung aller Faktoren. Die zuverlässigste Methode ist die Untersuchung der Betriebshistorie der Einrichtung.
Kriterien

Derzeit werden verschiedene Korrosionsraten in der Konstruktion verwendet:
- Nach der direkten Bewertungsmethode: Verringerung der Masse eines Metallteils pro Flächeneinheit - Gewichtsindikator (gemessen in Gramm pro 1 m2 für 1 Stunde); Schadenstiefe (oder Durchlässigkeit des Korrosionsprozesses), mm/Jahr; die Menge der freigesetzten Gasphase von Korrosionsprodukten; die Zeitspanne, während der die ersten Korrosionsschäden auftreten; Anzahl der Korrosionszentren pro FlächeneinheitOberflächen, die über einen bestimmten Zeitraum erschienen sind.
- Indirekt geschätzt: elektrochemische Korrosionsstromstärke; elektrischer Wiederstand; Veränderung der physikalischen und mechanischen Eigenschaften.
Der erste direkte Bewertungsindikator ist der häufigste.
Rechenformeln
Im allgemeinen Fall wird der Gewichtsverlust, der die Korrosionsrate des Metalls bestimmt, durch die folgende Formel gefunden:
Vkp=q/(St), wobei q die Abnahme der Masse des Metalls ist, g;
S - Fläche, von der das Material übertragen wurde, m2;
t - Zeitraum, Stunden
Bestimmen Sie für Bleche und daraus hergestellte Schalen den Tiefenindex (mm/Jahr):
H=m/t, m ist die Eindringtiefe in das Metall.
Zwischen dem ersten und dem zweiten oben beschriebenen Indikator besteht folgender Zusammenhang:
H=8, 76Vkp/ρ, wobei ρ die Dichte des Materials ist.
Hauptfaktoren, die die Korrosionsrate beeinflussen
Die folgenden Gruppen von Faktoren beeinflussen die Geschwindigkeit der Metallzerstörung:
- intern, bezogen auf die physikalische und chemische Natur des Materials (Phasenstruktur, chemische Zusammensetzung, Oberflächenrauheit des Teils, Rest- und Betriebsspannungen im Material und andere);
- extern (Umgebungsbedingungen, Bewegungsgeschwindigkeit eines korrosiven Mediums, Temperatur, Zusammensetzung der Atmosphäre, Vorhandensein von Hemmstoffen oder Stimulanzien und andere);
- mechanisch (Entstehung von Korrosionsrissen, Zerstörung von Metall unter Einwirkung zyklischer Belastungen,Kavitation und Passungskorrosion);
- Konstruktionsmerkmale (Auswahl der Metallsorte, Lücken zwischen den Teilen, Rauheitsanforderungen).
Physikalische und chemische Eigenschaften
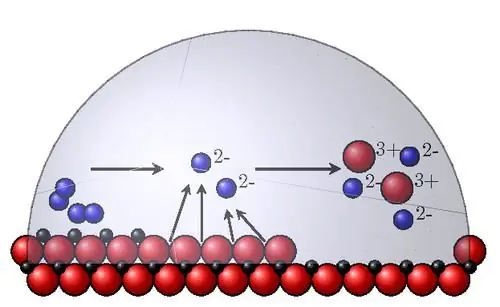
Die wichtigsten internen Korrosionsfaktoren sind die folgenden:
- Thermodynamische Stabilität. Zur Bestimmung in wässrigen Lösungen werden Referenz-Pourbaix-Diagramme verwendet, auf deren Abszissenachse der pH-Wert des Mediums und auf der Ordinate das Redoxpotential aufgetragen ist. Eine Potenzialverschiebung in die positive Richtung bedeutet eine größere Stabilität des Materials. Vorläufig wird es als das normale Gleichgewichtspotential des Metalls definiert. In Wirklichkeit korrodieren Materialien unterschiedlich schnell.
- Die Position eines Atoms im Periodensystem der chemischen Elemente. Die korrosionsanfälligsten Metalle sind Alkali- und Erdalkalimetalle. Die Korrosionsgeschwindigkeit nimmt mit zunehmender Ordnungszahl ab.
- Kristallstruktur. Es hat eine zweideutige Wirkung auf die Zerstörung. Das grobkörnige Gefüge selbst führt nicht zu einer Korrosionssteigerung, ist aber günstig für die Ausbildung einer interkristallinen selektiven Zerstörung von Korngrenzen. Metalle und Legierungen mit einer homogenen Phasenverteilung korrodieren gleichmäßig, während solche mit einer ungleichmäßigen Verteilung nach einem Fokusmechanismus korrodieren. Die gegenseitige Anordnung der Phasen übernimmt in aggressiver Umgebung die Funktion von Anode und Kathode.
- Energieinhomogenität von Atomen im Kristallgitter. Atome mit der höchsten Energie befinden sich an den Ecken der FlächenMikrorauhigkeiten und sind aktive Auflösungszentren bei chemischer Korrosion. Daher erhöht eine sorgfältige Bearbeitung von Metallteilen (Schleifen, Polieren, Finishen) die Korrosionsbeständigkeit. Dieser Effekt erklärt sich auch durch die Bildung dichterer und geschlossenerer Oxidschichten auf glatten Oberflächen.
Einfluss mittlerer Säuregeh alt

Bei der chemischen Korrosion beeinflusst die Konzentration von Wasserstoffionen die folgenden Punkte:
- Löslichkeit von Korrosionsprodukten;
- Bildung schützender Oxidschichten;
- Metallzerstörungsrate.
Wenn der pH-Wert im Bereich von 4-10 Einheiten (saure Lösung) liegt, hängt die Korrosion von Eisen von der Intensität des Eindringens von Sauerstoff an die Oberfläche des Objekts ab. In alkalischen Lösungen nimmt die Korrosionsrate zunächst durch Oberflächenpassivierung ab und steigt dann bei pH >13 durch Auflösung der schützenden Oxidschicht an.
Für jede Metallart gibt es eine eigene Abhängigkeit der Zerstörungsintensität vom Säuregrad der Lösung. Edelmetalle (Pt, Ag, Au) sind in saurer Umgebung korrosionsbeständig. Zn, Al werden sowohl in Säuren als auch in Laugen schnell zerstört. Ni und Cd sind beständig gegen Laugen, korrodieren jedoch leicht in Säuren.
Zusammensetzung und Konzentration neutraler Lösungen

Die Korrosionsgeschwindigkeit in neutralen Lösungen hängt mehr von den Eigenschaften des Salzes und seiner Konzentration ab:
- Während der Hydrolyse von Salzen inIn einer korrosiven Umgebung werden Ionen gebildet, die als Aktivatoren oder Verzögerer (Inhibitoren) der Metallzerstörung wirken.
- Die Verbindungen, die den pH-Wert erhöhen, erhöhen auch die Geschwindigkeit des destruktiven Prozesses (z. B. Soda), und diejenigen, die den Säuregeh alt verringern (Ammoniumchlorid).
- In Gegenwart von Chloriden und Sulfaten in der Lösung wird die Zerstörung aktiviert, bis eine bestimmte Konzentration von Salzen erreicht ist (was durch die Intensivierung des Anodenprozesses unter dem Einfluss von Chlorid- und Schwefelionen erklärt wird), und nimmt dann aufgrund einer Abnahme der Sauerstofflöslichkeit allmählich ab.
Einige Arten von Salzen können einen unlöslichen Film bilden (z. B. Eisenphosphat). Dies trägt dazu bei, das Metall vor weiterer Zerstörung zu schützen. Diese Eigenschaft wird beim Auftragen von Rostneutralisatoren genutzt.
Korrosionsschutzmittel
Korrosionsinhibitoren (oder Inhibitoren) unterscheiden sich in ihrem Wirkungsmechanismus auf den Redoxprozess:
- Anode. Dank ihnen wird ein passiver Film gebildet. Zu dieser Gruppe gehören Verbindungen auf Basis von Chromaten und Bichromaten, Nitraten und Nitriten. Die letzte Art von Inhibitoren wird zum interoperativen Schutz von Teilen verwendet. Beim Einsatz von anodischen Korrosionsinhibitoren ist zunächst deren Mindestschutzkonzentration zu ermitteln, da die Zugabe geringer Mengen zu einer Erhöhung der Abtötungsgeschwindigkeit führen kann.
- Kathode. Der Mechanismus ihrer Wirkung beruht auf einer Abnahme der Sauerstoffkonzentration und dementsprechend einer Verlangsamung des kathodischen Prozesses.
- Abschirmung. Diese Inhibitoren isolieren die Metalloberfläche, indem sie unlösliche Verbindungen bilden, die sich als Schutzschicht ablagern.
Zur letzten Gruppe gehören Rostneutralisatoren, die auch zur Reinigung von Oxiden verwendet werden. Sie enth alten normalerweise Phosphorsäure. Unter seinem Einfluss tritt eine Metallphosphatierung auf - die Bildung einer starken Schutzschicht aus unlöslichen Phosphaten. Neutralisatoren werden mit einer Spritzpistole oder Rolle aufgetragen. Nach 25-30 Minuten nimmt die Oberfläche eine weißgraue Farbe an. Nachdem die Zusammensetzung getrocknet ist, werden Farben und Lacke aufgetragen.
Mechanik

Ein Anstieg der Korrosion in einer aggressiven Umgebung wird durch mechanische Einwirkungen begünstigt wie:
- Interne (während des Formens oder der Wärmebehandlung) und externe (unter dem Einfluss einer von außen aufgebrachten Last) Spannungen. Infolgedessen tritt eine elektrochemische Inhomogenität auf, die thermodynamische Stabilität des Materials nimmt ab und es bilden sich Korrosionsrisse. Besonders schnell erfolgt die Zerstörung bei Zugbelastung (Risse bilden sich in senkrechten Ebenen) in Gegenwart von oxidierenden Anionen, zB NaCl. Ein typisches Beispiel für Geräte, die dieser Art der Zerstörung unterliegen, sind Teile von Dampfkesseln.
- Wechselschwingung, Vibration (Korrosionsermüdung). Es kommt zu einer intensiven Abnahme der Ermüdungsgrenze, es bilden sich mehrere Mikrorisse, die dann zu einem großen verschmelzen. AnzahlZyklen bis zum Versagen hängt in größerem Maße von der chemischen und Phasenzusammensetzung von Metallen und Legierungen ab. Pumpenachsen, Federn, Turbinenschaufeln und andere Ausrüstung sind dieser Korrosion ausgesetzt.
- Reibung von Teilen. Schnelle Korrosion ist auf mechanischen Verschleiß der Schutzfilme auf der Oberfläche des Teils und chemische Wechselwirkung mit der Umgebung zurückzuführen. In Flüssigkeit ist die Zerstörungsrate geringer als in Luft.
- Kavitationseinfluss. Kavitation tritt auf, wenn die Kontinuität des Flüssigkeitsstroms durch die Bildung von Vakuumblasen unterbrochen wird, die zusammenbrechen und einen pulsierenden Effekt erzeugen. Infolgedessen treten tiefe Schäden lokaler Natur auf. Diese Art von Korrosion wird häufig in chemischen Apparaten beobachtet.
Designfaktoren

Bei der Konstruktion von Elementen, die unter aggressiven Bedingungen betrieben werden, muss berücksichtigt werden, dass die Korrosionsrate in folgenden Fällen ansteigt:
- wenn ungleiche Metalle in Kontakt kommen (je größer der Unterschied im Elektrodenpotential zwischen ihnen ist, desto höher ist die Stromstärke des elektrochemischen Zerstörungsprozesses);
- in Gegenwart von mechanischen Spannungskonzentratoren (Rillen, Rillen, Löcher und andere);
- mit geringer Sauberkeit der bearbeiteten Oberfläche, da dies zu lokalen kurzgeschlossenen galvanischen Paaren führt;
- bei erheblichem Temperaturunterschied einzelner Geräteteile (es bilden sich thermisch galvanische Zellen);
- bei Vorhandensein von stagnierenden Zonen (Schlitze, Lücken);
- beim FormenRestspannungen, insbesondere in Schweißverbindungen (um sie zu beseitigen, ist eine Wärmebehandlung - Glühen) vorzusehen.
Bewertungsmethoden

Es gibt mehrere Möglichkeiten, die Zerstörungsrate von Metallen in aggressiven Umgebungen zu bestimmen:
- Labor - Testen von Proben unter künstlich simulierten Bedingungen, die der Realität nahe kommen. Ihr Vorteil ist, dass sie es Ihnen ermöglichen, die Studienzeit zu verkürzen.
- Feld - findet unter natürlichen Bedingungen statt. Sie brauchen lange. Der Vorteil dieser Methode besteht darin, Informationen über die Eigenschaften des Metalls unter den Bedingungen des weiteren Betriebs zu erh alten.
- In-situ-Tests von fertigen Metallobjekten in der natürlichen Umgebung.






