Der dreidimensionale Zustand von flüssigem Wasser ist schwer zu untersuchen, aber durch die Analyse der Struktur von Eiskristallen wurde viel gelernt. Vier benachbarte, mit Wasserstoff wechselwirkende Sauerstoffatome besetzen die Eckpunkte eines Tetraeders (Tetra=vier, Hedron=Ebene). Die durchschnittliche Energie, die erforderlich ist, um eine solche Bindung in Eis zu brechen, wird auf 23 kJ/mol geschätzt-1.

Die Fähigkeit von Wassermolekülen, eine bestimmte Anzahl von Wasserstoffketten sowie eine bestimmte Stärke zu bilden, erzeugt einen ungewöhnlich hohen Schmelzpunkt. Wenn es schmilzt, wird es von flüssigem Wasser geh alten, dessen Struktur unregelmäßig ist. Die meisten Wasserstoffbrückenbindungen sind verzerrt. Es braucht viel Energie in Form von Wärme, um das Kristallgitter von wasserstoffgebundenem Eis aufzubrechen.
Merkmale des Aussehens von Eis (Ih)
Viele Einwohner fragen sich, was für ein Kristallgitter Eis hat. NotwendigEs sollte beachtet werden, dass die Dichte der meisten Substanzen während des Gefrierens zunimmt, wenn sich die Molekülbewegungen verlangsamen und sich dicht gepackte Kristalle bilden. Auch die Dichte von Wasser nimmt zu, wenn es auf maximal 4°C (277K) abkühlt. Wenn die Temperatur dann unter diesen Wert fällt, dehnt es sich aus.
Dieser Anstieg ist auf die Bildung eines offenen, wasserstoffgebundenen Eiskristalls mit seinem Gitter und geringerer Dichte zurückzuführen, in dem jedes Wassermolekül durch das obige Element und vier andere Werte starr gebunden ist, während es sich schnell genug bewegt mehr Masse haben. Da dieser Vorgang auftritt, gefriert die Flüssigkeit von oben nach unten. Dies hat wichtige biologische Auswirkungen, wodurch die Eisschicht auf dem Teich Lebewesen vor extremer Kälte schützt. Darüber hinaus hängen zwei weitere Eigenschaften von Wasser mit seinen Wasserstoffeigenschaften zusammen: spezifische Wärme und Verdunstung.
Ausführliche Strukturbeschreibung
Das erste Kriterium ist die Menge, die benötigt wird, um die Temperatur von 1 Gramm einer Substanz um 1°C zu erhöhen. Die Erhöhung des Wassergrades erfordert relativ viel Wärme, da jedes Molekül an zahlreichen Wasserstoffbrückenbindungen beteiligt ist, die aufgebrochen werden müssen, damit die kinetische Energie zunimmt. Übrigens, die Fülle von H2O in den Zellen und Geweben aller großen vielzelligen Organismen bedeutet, dass Temperaturschwankungen innerhalb der Zellen minimiert werden. Dieses Merkmal ist entscheidend, da die Geschwindigkeit der meisten biochemischen Reaktionensensibel.
Auch die Verdampfungswärme von Wasser ist deutlich höher als die vieler anderer Flüssigkeiten. Um diesen Körper in ein Gas umzuwandeln, ist eine große Wärmemenge erforderlich, da die Wasserstoffbrückenbindungen aufgebrochen werden müssen, damit sich die Wassermoleküle voneinander lösen und in die genannte Phase eintreten können. Veränderliche Körper sind permanente Dipole und können mit anderen ähnlichen Verbindungen und solchen, die ionisieren und sich auflösen, interagieren.
Andere oben genannte Stoffe können nur bei vorhandener Polarität in Kontakt kommen. Es ist diese Verbindung, die an der Struktur dieser Elemente beteiligt ist. Außerdem kann es sich um diese aus Elektrolyten gebildeten Partikel anordnen, sodass die negativen Sauerstoffatome der Wassermoleküle zu den Kationen und die positiven Ionen und Wasserstoffatome zu den Anionen orientiert sind.
In Festkörpern werden in der Regel molekulare und atomare Kristallgitter gebildet. Das heißt, wenn Jod so aufgebaut ist, dass es I2, enthält, dann sind in festem Kohlendioxid, also in Trockeneis, CO2-Moleküle enth alten befindet sich an den Kristallgitterknoten . Bei der Wechselwirkung mit ähnlichen Substanzen hat Eis ein ionisches Kristallgitter. Graphit zum Beispiel, das eine auf Kohlenstoff basierende atomare Struktur hat, ist nicht in der Lage, diese zu verändern, genau wie Diamant.
Was passiert, wenn sich ein Kochsalzkristall in Wasser auflöst: Polare Moleküle werden von geladenen Elementen im Kristall angezogen, was zur Bildung ähnlicher Natrium- und Chloridpartikel auf seiner Oberfläche führt, was zu diesen Körpern führtwerden voneinander getrennt, und es beginnt sich aufzulösen. Von hier aus kann beobachtet werden, dass Eis ein Kristallgitter mit ionischer Bindung hat. Jedes gelöste Na + zieht die negativen Enden mehrerer Wassermoleküle an, während jedes gelöste Cl - die positiven Enden anzieht. Die Hülle, die jedes Ion umgibt, wird Fluchtkugel genannt und enthält normalerweise mehrere Schichten von Lösungsmittelpartikeln.
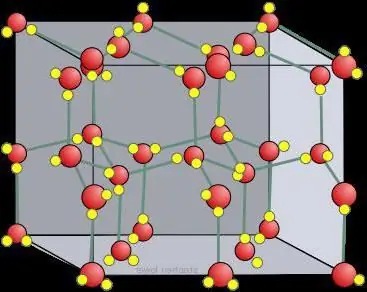
Trockeneiskristallgitter
Variablen oder ein Ion, das von Elementen umgeben ist, nennt man sulfatiert. Wenn das Lösungsmittel Wasser ist, werden solche Teilchen hydratisiert. Somit neigt jedes polare Molekül dazu, durch die Elemente des flüssigen Körpers solvatisiert zu werden. Im Trockeneis bildet die Art des Kristallgitters im Aggregatzustand Atombindungen, die unverändert bleiben. Eine andere Sache ist kristallines Eis (gefrorenes Wasser). Ionische organische Verbindungen wie Carboxylase und protonierte Amine müssen in Hydroxyl- und Carbonylgruppen löslich sein. Die in solchen Strukturen enth altenen Teilchen bewegen sich zwischen Molekülen, und ihre polaren Systeme bilden Wasserstoffbrücken mit diesem Körper.
Natürlich beeinflusst die Anzahl der zuletzt angegebenen Gruppen in einem Molekül seine Löslichkeit, die auch von der Reaktion verschiedener Strukturen im Element abhängt: Beispielsweise sind Ein-, Zwei- und Drei-Kohlenstoff-Alkohole mischbar mit Wasser, aber größere Kohlenwasserstoffe mit einzelnen Hydroxylverbindungen sind in Flüssigkeiten viel weniger verdünnt.
Hexagonal Ih hat eine ähnliche Form wieAtomkristallgitter. Für Eis und allen natürlichen Schnee auf der Erde sieht es genau so aus. Dies wird durch die Symmetrie des Kristallgitters von Eis belegt, das aus Wasserdampf (dh Schneeflocken) gewachsen ist. Es ist in Raumgruppe P 63/mm von 194; D 6h, Laue-Klasse 6/mm; ähnlich wie β-, das ein Vielfaches von 6 Schraubenachse hat (Rotation um zusätzlich zu Verschiebung entlang). Es hat eine ziemlich offene Struktur mit geringer Dichte, bei der die Effizienz im Vergleich zu einfachen kubischen (~1/2) oder flächenzentrierten kubischen (~3/4) Strukturen gering ist (~1/3).
Im Vergleich zu gewöhnlichem Eis ist das Kristallgitter von Trockeneis, gebunden durch CO2 Moleküle, statisch und ändert sich nur, wenn Atome zerfallen.
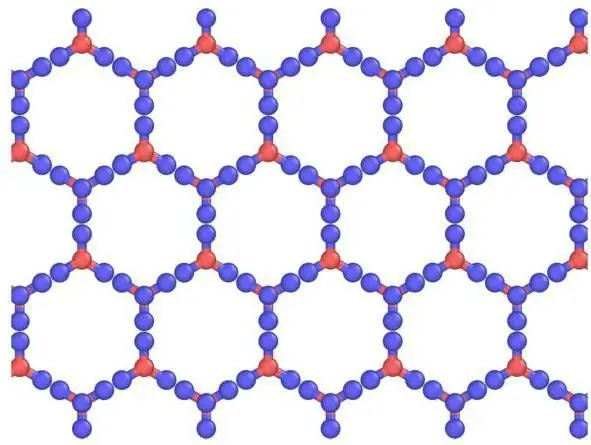
Beschreibung der Gitter und ihrer Elemente
Kristalle können als kristalline Modelle betrachtet werden, die aus übereinander gelegten Schichten bestehen. Die Wasserstoffbrückenbindung ist geordnet, während sie in Wirklichkeit zufällig ist, da sich Protonen bei Temperaturen über etwa 5 K zwischen Wasser-(Eis-)Molekülen bewegen können. In der Tat ist es wahrscheinlich, dass sich Protonen wie eine Quantenflüssigkeit in einem konstanten Tunnelfluss verh alten. Dies wird durch die Streuung von Neutronen verstärkt, die ihre Streudichte auf halbem Weg zwischen den Sauerstoffatomen zeigt, was auf eine Lokalisierung und konzertierte Bewegung hinweist. Hier besteht eine Ähnlichkeit von Eis mit einem atomaren, molekularen Kristallgitter.
Moleküle haben eine versetzte Anordnung der Wasserstoffkettein Bezug auf seine drei Nachbarn in der Ebene. Das vierte Element hat eine verdunkelte Anordnung von Wasserstoffbrückenbindungen. Es gibt eine leichte Abweichung von der perfekten hexagonalen Symmetrie, da die Einheitszelle in Richtung dieser Kette um 0,3 % kürzer ist. Alle Moleküle erfahren dieselben molekularen Umgebungen. In jeder "Box" ist genügend Platz, um interstitielle Wasserpartikel aufzunehmen. Obwohl nicht allgemein in Betracht gezogen, wurden sie kürzlich durch Neutronenbeugung des pulverförmigen Kristallgitters von Eis effektiv nachgewiesen.
Wechselsubstanzen
Der sechseckige Körper hat Tripelpunkte mit flüssigem und gasförmigem Wasser 0,01 °C, 612 Pa, feste Elemente - drei -21,985 °C, 209,9 MPa, elf und zwei -199,8 °C, 70 MPa, sowie - 34,7 °C, 212,9 MPa. Die Dielektrizitätskonstante von hexagonalem Eis beträgt 97,5.
Die Schmelzkurve dieses Elements ist in MPa angegeben. Die Zustandsgleichungen sind verfügbar, zusätzlich dazu einige einfache Ungleichungen, die die Änderung der physikalischen Eigenschaften mit der Temperatur von hexagonalem Eis und seinen wässrigen Suspensionen in Beziehung setzen. Die Härte schwankt mit zunehmendem Grad von oder unter Gips (≦2) bei 0 °C bis Feldspat (6 Mohs) bei -80 °C, eine ungewöhnlich große Änderung der absoluten Härte (> 24-mal).
Das hexagonale Kristallgitter von Eis bildet hexagonale Platten und Säulen, wobei die oberen und unteren Flächen die Basalebenen {0 0 0 1} mit einer Enthalpie von 5,57 μJ cm -2 sindund andere äquivalente Seitenteile werden Teile des Prismas {1 0 -1 0} mit 5, 94 genanntµJ cm -2. Nebenflächen {1 1 -2 0} mit 6,90 ΜJ ˣ cm -2 können entlang der durch die Seiten der Strukturen gebildeten Ebenen gebildet werden.
Eine solche Struktur zeigt eine anomale Abnahme der Wärmeleitfähigkeit mit steigendem Druck (sowie kubisches und amorphes Eis geringer Dichte), unterscheidet sich aber von den meisten Kristallen. Das liegt an einer Veränderung der Wasserstoffbrückenbindung, die die Querschallgeschwindigkeit im Kristallgitter von Eis und Wasser reduziert.
Es gibt Methoden, die beschreiben, wie man große Kristallproben und jede gewünschte Eisoberfläche präpariert. Es wird angenommen, dass die Wasserstoffbrückenbindung auf der Oberfläche des untersuchten hexagonalen Körpers geordneter ist als innerhalb des Volumensystems. Variationsspektroskopie mit Phasengitter-Frequenzerzeugung hat gezeigt, dass es eine strukturelle Asymmetrie zwischen den beiden oberen Schichten (L1 und L2) in der unterirdischen HO-Kette der basalen Oberfläche von hexagonalem Eis gibt. Die angenommenen Wasserstoffbrückenbindungen in den oberen Schichten der Sechsecke (L1 O ··· HO L2) sind stärker als die angenommenen in der zweiten Schicht zur oberen Ansammlung (L1 OH ··· O L2). Interaktive sechseckige Eisstrukturen verfügbar.
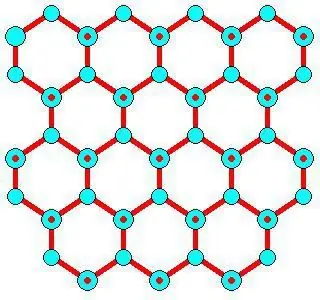
Entwicklungsfunktionen
Die Mindestanzahl an Wassermolekülen, die zur Bildung von Eis benötigt wird, beträgt ungefähr 275 ± 25, wie für einen vollständigen ikosaedrischen Cluster von 280. Die Bildung erfolgt mit einer Geschwindigkeit von 10 10 am Luft-Wasser-Grenzfläche und nicht in Massenwasser. Das Wachstum von Eiskristallen hängt von verschiedenen Wachstumsraten abEnergien. Bei der Kryokonservierung von biologischen Proben, Lebensmitteln und Organen muss das Wasser vor dem Gefrieren geschützt werden.
Dies wird typischerweise durch schnelle Abkühlungsraten erreicht, indem kleine Proben und ein Kryokonservator verwendet werden und der Druck erhöht wird, um Eis zu nukleieren und Zellschäden zu verhindern. Die freie Energie von Eis/Flüssigkeit steigt von ~30 mJ/m2 bei atmosphärischem Druck auf 40 mJ/m-2 bei 200 MPa an, was anzeigt Grund, warum dieser Effekt auftritt.
Welche Art von Kristallgitter ist charakteristisch für Eis
Alternativ können sie schneller von Prismenoberflächen (S2) auf der zufällig gestörten Oberfläche von schnellgefrorenen oder bewegten Seen wachsen. Das Wachstum von den {1 1 -2 0}-Flächen ist mindestens gleich, verwandelt sie aber in Prismenbasen. Die Daten zur Entwicklung des Eiskristalls sind vollständig untersucht. Die relativen Wachstumsraten von Elementen verschiedener Flächen hängen von der Fähigkeit ab, ein hohes Maß an gemeinsamer Hydratation zu bilden. Die Temperatur (niedrig) des umgebenden Wassers bestimmt den Verzweigungsgrad im Eiskristall. Das Partikelwachstum wird durch die Diffusionsrate bei einem niedrigen Unterkühlungsgrad, dh <2 ° C, begrenzt, was zu mehr Partikeln führt.

Aber begrenzt durch die Entwicklungskinetik bei höheren Depressionsniveaus von >4°C, was zu Nadelwachstum führt. Diese Form ähnelt der Struktur von Trockeneis (hat ein Kristallgitter mit einer sechseckigen Struktur), verschiedeneEigenschaften der Oberflächenentwicklung und der Temperatur des umgebenden (unterkühlten) Wassers, das sich hinter den flachen Formen der Schneeflocken befindet.
Die Bildung von Eis in der Atmosphäre beeinflusst die Bildung und Eigenschaften von Wolken grundlegend. Feldspäte, die im Wüstenstaub vorkommen, der jährlich in Millionen Tonnen in die Atmosphäre gelangt, sind wichtige Bildner. Computersimulationen haben gezeigt, dass dies auf die Keimbildung von prismatischen Eiskristallebenen auf hochenergetischen Oberflächenebenen zurückzuführen ist.
Einige andere Elemente und Gitter
Gelöste Substanzen (mit Ausnahme von sehr kleinem Helium und Wasserstoff, die in die Zwischenräume eindringen können) können bei atmosphärischem Druck nicht in die Ih-Struktur eingeschlossen werden, sondern werden an die Oberfläche oder amorphe Schicht zwischen den Partikeln des gebildet Mikrokristalliner Körper. An den Gitterplätzen des Trockeneises befinden sich noch einige andere Elemente: chaotrope Ionen wie NH4 + und Cl -, die in leichterem flüssigem Einfrieren enth alten sind als andere kosmotrope wie Na + und SO42-, daher ist es nicht möglich, sie zu entfernen, da sie einen dünnen Film der verbleibenden Flüssigkeit zwischen den Kristallen bilden. Dies kann zu einer elektrischen Aufladung der Oberfläche durch Dissoziation des Oberflächenwassers führen, die die verbleibenden Ladungen ausgleicht (was auch zu einer magnetischen Strahlung führen kann) und zu einer Änderung des pH-Werts der verbleibenden Flüssigkeitsfilme, z. B. NH 42SO4 wird saurer und NaCl wird basischer.
Sie stehen senkrecht zu den FlächenKristallgitter aus Eis, das die nächste angelagerte Schicht zeigt (mit O-Atomen in Schwarz). Sie zeichnen sich durch eine langsam wachsende Grundfläche {0 0 0 1} aus, an der nur vereinzelt Wassermoleküle angelagert sind. Eine schnell wachsende {1 0 -1 0}-Fläche eines Prismas, an der sich Paare neu angelagerter Teilchen mit Wasserstoff verbinden können (eine Wasserstoffbrücke/zwei Moleküle eines Elements). Die am schnellsten wachsende Fläche ist {1 1 -2 0} (sekundäres Prisma), wo Ketten neu angelagerter Teilchen durch Wasserstoffbrückenbindungen miteinander wechselwirken können. Eine ihrer Ketten/Elementmoleküle ist eine Form, die Grate bildet, die die Umwandlung in zwei Seiten des Prismas teilen und fördern.
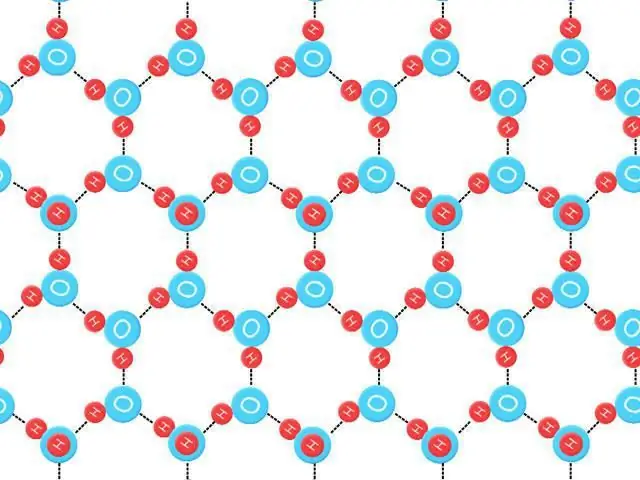
Nullpunktsentropie
Kann definiert werden als S 0=k B ˣ Ln (N E0), wobei k B die Boltzmann-Konstante, NE die Anzahl der Konfigurationen bei der Energie E und E0 die niedrigste Energie ist. Dieser Wert für die Entropie von hexagonalem Eis bei null Kelvin verstößt nicht gegen den dritten Hauptsatz der Thermodynamik „Die Entropie eines idealen Kristalls am absoluten Nullpunkt ist genau null“, da diese Elemente und Teilchen nicht ideal sind, ungeordnete Wasserstoffbrückenbindungen haben.
In diesem Körper ist die Wasserstoffbrücke zufällig und ändert sich schnell. Diese Strukturen sind energetisch nicht exakt gleich, sondern erstrecken sich auf eine sehr große Zahl von energetisch nahen Zuständen, gehorchen den "Regeln des Eises". Die Nullpunktsentropie ist die Unordnung, die bestehen bleiben würde, selbst wenn das Material bis zum absoluten Grad abgekühlt werden könnteNull (0 K=-273, 15 ° C). Erzeugt experimentelle Verwirrung für hexagonales Eis 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1. Theoretisch wäre es möglich, die Nullentropie bekannter Eiskristalle mit viel größerer Genauigkeit zu berechnen (unter Vernachlässigung von Defekten und Energieniveaustreuung), als sie experimentell zu bestimmen.
Wissenschaftler und ihre Arbeit auf diesem Gebiet
Kann definiert werden als S 0=k B ˣ Ln (N E0), wobei k B die Boltzmann-Konstante, NE die Anzahl der Konfigurationen bei der Energie E und E0 die niedrigste Energie ist. Dieser Wert für die Entropie von hexagonalem Eis bei null Kelvin verstößt nicht gegen den dritten Hauptsatz der Thermodynamik „Die Entropie eines idealen Kristalls am absoluten Nullpunkt ist genau null“, da diese Elemente und Teilchen nicht ideal sind, ungeordnete Wasserstoffbrückenbindungen haben.
In diesem Körper ist die Wasserstoffbrücke zufällig und ändert sich schnell. Diese Strukturen sind energetisch nicht exakt gleich, sondern erstrecken sich auf eine sehr große Zahl von energetisch nahen Zuständen, gehorchen den "Regeln des Eises". Die Nullpunktsentropie ist die Unordnung, die bestehen bleiben würde, selbst wenn das Material auf den absoluten Nullpunkt (0 K=-273,15 °C) abgekühlt werden könnte. Erzeugt experimentelle Verwirrung für hexagonales Eis 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1. Theoretisch wäre es möglich, die Nullentropie bekannter Eiskristalle mit viel größerer Genauigkeit zu berechnen (unter Vernachlässigung von Defekten und Energieniveaustreuung), als sie experimentell zu bestimmen.

Obwohl die Anordnung der Protonen im Eis nicht geordnet ist, bevorzugt die Oberfläche wahrscheinlich die Anordnung dieser Teilchen in Form von Bändern aus hängenden H-Atomen und O-Einzelpaaren (Null-Entropie mit geordneten Wasserstoffbrückenbindungen). Die Nullpunktsstörung ZPE, J ˣ mol -1 ˣ K -1 und andere wird gefunden. Aus all dem ist klar und verständlich, welche Arten von Kristallgittern für Eis charakteristisch sind.






