In unserer Zeit ist die Physik zu einer sehr verbreiteten Wissenschaft geworden. Es ist buchstäblich überall präsent. Das elementarste Beispiel: In Ihrem Garten wächst ein Apfelbaum, und darauf reifen Früchte, die Zeit kommt und die Äpfel beginnen zu fallen, aber in welche Richtung fallen sie? Dank des universellen Gravitationsgesetzes fällt unser Fötus zu Boden, das heißt, er geht nach unten, aber nicht nach oben. Es war eines der berühmtesten Beispiele der Physik, aber widmen wir uns der Thermodynamik, genauer gesagt den Phasengleichgewichten, die in unserem Leben nicht weniger wichtig sind.
Thermodynamik

Sehen wir uns zunächst diesen Begriff an. ΘερΜοδυναΜική - so sieht das Wort auf Griechisch aus. Der erste Teil ΘερΜo bedeutet "Wärme" und der zweite δυναΜική bedeutet "Stärke". Die Thermodynamik ist ein Zweig der Physik, der die Eigenschaften eines makroskopischen Systems sowie verschiedene Arten der Umwandlung und Übertragung von Energie untersucht. In diesem Abschnitt werden verschiedene Zustände und Prozesse speziell untersucht, damit der Begriff der Temperatur in die Beschreibung eingeführt werden kann (dies ist eine physikalische Größe, die ein thermodynamisches System charakterisiert und gemessen wird mitbestimmte Geräte). Alle ablaufenden Prozesse in thermodynamischen Systemen werden nur durch mikroskopische Größen (Druck und Temperatur sowie die Konzentration von Bestandteilen) beschrieben.
Clapeyron-Clausius-Gleichung
Jeder Physiker kennt diese Gleichung, aber lass sie uns Stück für Stück aufschlüsseln. Es bezieht sich auf die Gleichgewichtsprozesse des Übergangs bestimmter Materie von einer Phase in eine andere. Dies ist an solchen Beispielen deutlich zu sehen: Schmelzen, Verdampfen, Sublimation (eine der Möglichkeiten, Produkte zu konservieren, die durch vollständigen Entzug von Feuchtigkeit erfolgt). Die Formel zeigt deutlich die laufenden Prozesse:
- n=PV/RT;
- wobei T die Temperatur der Substanz ist;
- P-Druck;
- R-spezifische Phasenübergangswärme;
- V-Änderung in spezifischer Lautstärke.
Die Entstehungsgeschichte der Gleichung

Die Clausius-Clapeyron-Gleichung ist eine ausgezeichnete mathematische Erklärung des zweiten Hauptsatzes der Thermodynamik. Auch als "Clausius-Ungleichung" bezeichnet. Das Theorem wurde natürlich von dem Wissenschaftler selbst entwickelt, der den Zusammenhang zwischen dem Wärmefluss im System und der Entropie sowie seiner Umgebung erklären wollte. Diese Gleichung wurde von Clausius bei seinen Versuchen entwickelt, die Entropie zu erklären und zu quantifizieren. Im wörtlichen Sinne gibt uns der Satz die Möglichkeit zu bestimmen, ob ein Kreisprozess reversibel oder irreversibel ist. Diese Ungleichung bietet uns eine quantitative Formel zum Verständnis des zweiten Hauptsatzes.
Der Wissenschaftler war einer der ersten, der sich mit der Idee der Entropie beschäftigte und sie sogar gabProzessname. Was heute als Satz von Clausius bekannt ist, wurde erstmals 1862 in Rudolfs sechstem Werk Über die Verwendung des Transformationsäquivalenzsatzes für Innenarbeiten veröffentlicht. Der Wissenschaftler versuchte, einen proportionalen Zusammenhang zwischen Entropie und Energiefluss durch Erwärmung (δ Q) im System aufzuzeigen. Beim Bauen kann diese thermische Energie in Arbeit umgewandelt und durch einen Kreisprozess in Wärme umgewandelt werden. Rudolph bewies, dass „die algebraische Summe aller in einem Kreisprozess auftretenden Transformationen nur kleiner Null oder im Extremfall gleich Null sein kann.“
Geschlossenes Inselsystem
Isoliertes System ist eines der folgenden:
- Physisches System ist weit entfernt von anderen, die nicht mit ihnen interagieren.
- Das thermodynamische System ist durch starre, unbewegliche Wände abgeschlossen, durch die weder Materie noch Energie passieren können.
Trotz der Tatsache, dass das Subjekt innerlich mit seiner eigenen Schwerkraft verbunden ist, wird ein isoliertes System normalerweise über die Grenzen der äußeren Gravitation und anderer entfernter Kräfte hinausgeführt.
Dies steht im Gegensatz zu dem, was (in der allgemeineren Terminologie der Thermodynamik) ein geschlossenes System genannt wird, das von selektiven Wänden umgeben ist, durch die Energie in Form von Wärme oder Arbeit übertragen werden kann, aber keine Materie. Und mit einem offenen System, in das Materie und Energie eintreten oder austreten, obwohl es verschiedene undurchdringliche Wände darin haben kannTeile seiner Grenzen.
Ein isoliertes System gehorcht dem Erh altungssatz. Meistens werden in der Thermodynamik Materie und Energie als getrennte Konzepte betrachtet.
Thermodynamische Übergänge
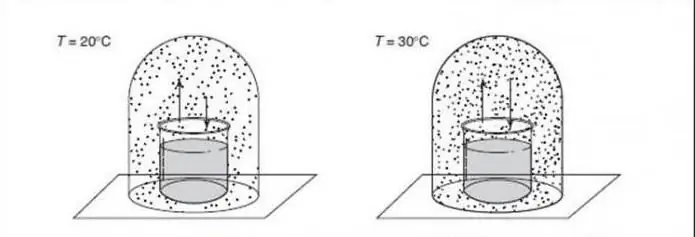
Um Quantenphasenübergänge zu verstehen, ist es hilfreich, sie mit klassischen Transformationen (auch thermische Inversionen genannt) zu vergleichen. CPT beschreibt die Spitze in den thermodynamischen Eigenschaften eines Systems. Es signalisiert die Reorganisation von Partikeln. Ein typisches Beispiel ist der Gefrierübergang von Wasser, der einen fließenden Übergang zwischen einer Flüssigkeit und einem Feststoff beschreibt. Klassisches Phasenwachstum beruht auf der Konkurrenz zwischen der Energie des Systems und der Entropie seiner thermischen Fluktuationen.
Ein klassisches System hat bei Nulltemperatur keine Entropie und daher kann keine Phasenumwandlung stattfinden. Ihre Ordnung wird durch die erste diskontinuierliche Ableitung des thermodynamischen Potentials bestimmt. Und natürlich hat es die erste Ordnung. Phasentransformationen von einem Ferromagneten zu einem Paramagneten sind kontinuierlich und zweiter Ordnung. Diese ständigen Änderungen von einer geordneten zu einer ungeordneten Phase werden durch einen Ordnungsparameter beschrieben, der Null ist. Für die obige ferromagnetische Transformation ist der Ordnungsparameter die Gesamtmagnetisierung des Systems.
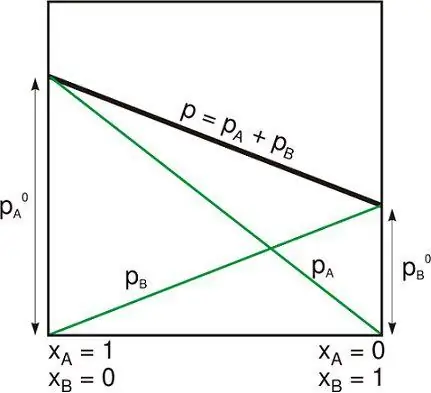
Gibbs-Potential
Die freie Gibbs-Energie ist die maximale Menge an Arbeit ohne Ausdehnung, die einem thermodynamisch geschlossenen System entnommen werden kann (das Wärme austauschen und mit der Umgebung arbeiten kann). Solchdas maximale Ergebnis kann nur in einem vollständig reversiblen Prozess erzielt werden. Wenn sich das System vom ersten Zustand in den zweiten zurückverwandelt, ist die Verringerung der freien Gibbs-Energie gleich der, die das System in seiner Umgebung verrichtet, abzüglich der Arbeit der Druckkräfte.
Gleichgewichtszustände

Thermodynamisches und mechanisches Gleichgewicht ist ein axiomatisches Konzept der Thermodynamik. Dies ist der innere Zustand eines oder mehrerer Systeme, die durch mehr oder weniger durchlässige oder undurchlässige Wände verbunden sind. In diesem Zustand gibt es keine reinen makroskopischen Materie- oder Energieflüsse, weder innerhalb eines Systems noch zwischen Systemen.
In seiner eigenen Vorstellung vom Zustand des inneren Gleichgewichts findet keine makroskopische Veränderung statt. Die Systeme befinden sich gleichzeitig in gegenseitigen thermischen, mechanischen, chemischen (konstanten) Strahlungsgleichgewichten. Sie können in der gleichen Form vorliegen. Bei diesem Vorgang werden alle Ansichten auf einmal und auf unbestimmte Zeit gespeichert, bis die physische Operation unterbrochen wird. Im makroskopischen Gleichgewicht findet ein vollkommen präziser, ausgewogener Austausch statt. Der obige Beweis ist eine physikalische Erklärung dieses Konzepts.
Grundlagen
Alle Gesetze, Theoreme, Formeln haben ihre eigenen Grundlagen. Schauen wir uns die 3 Grundlagen des Phasengleichgewichtsgesetzes an.
- Phase ist eine Form von Materie, homogen in chemischer Zusammensetzung, physikalischem Zustand und mechanischem Gleichgewicht. Typische Phasen sind fest, flüssig und gasförmig. Zwei nicht mischbare Flüssigkeiten (oder Flüssigkeitsgemische mit unterschiedlichen Zusammensetzungen), die durch eine separate Grenze getrennt sind, gelten als zwei unterschiedliche Phasen und nicht mischbare Feststoffe.
- Die Anzahl der Komponenten (C) ist die Anzahl der chemisch unabhängigen Komponenten des Systems. Die Mindestanzahl unabhängiger Arten, die erforderlich ist, um die Zusammensetzung aller Phasen des Systems zu bestimmen.
- Die Anzahl der Freiheitsgrade (F) ist in diesem Zusammenhang die Anzahl der intensiven Variablen, die voneinander unabhängig sind.
Klassifizierung nach Phasengleichgewichten
- Reaktionen des kontinuierlichen Nettotransfers (oft als Festkörperreaktionen bezeichnet) treten zwischen Feststoffen unterschiedlicher Zusammensetzung auf. Sie können Elemente enth alten, die in Flüssigkeiten vorkommen (H, C), aber diese Elemente werden in festen Phasen zurückgeh alten, sodass keine flüssigen Phasen als Reaktanten oder Produkte beteiligt sind (H2O, CO2). Reine Festkörperübertragungsreaktionen können kontinuierlich oder diskontinuierlich oder endständig sein.
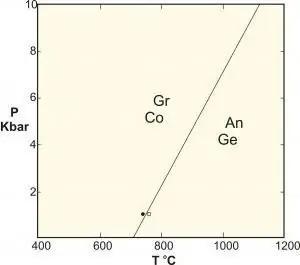
- Polymorphe sind eine spezielle Art der Festphasenreaktion, die Phasen identischer Zusammensetzung umfasst. Klassische Beispiele sind die Reaktionen zwischen Aluminiumsilikaten Kyanit-Sillimanit-Andalusit, die Umwandlung von Graphit in Diamant bei hohem Druck und das Gleichgewicht von Calciumcarbonat.
Gleichgewichtsgesetze

Die Gibbs-Factory-Regel wurde von Josiah Willard Gibbs in seinem berühmten Artikel mit dem Titel "The Equilibrium of Heterogeneous Substances" vorgeschlagen, der von 1875 bis 1878 erschien. Es gilt fürnicht reaktive heterogene Mehrkomponentensysteme im thermodynamischen Gleichgewicht und ist eine gegebene Gleichheit:
- F=C-P+2;
- wobei F die Anzahl der Freiheitsgrade ist;
- C - Anzahl der Komponenten;
- P - Anzahl der Phasen im thermodynamischen Gleichgewicht miteinander.
Die Anzahl der Freiheitsgrade ist die Anzahl der unbesetzten intensiven Variablen. Die größte Anzahl thermodynamischer Parameter wie Temperatur oder Druck, die gleichzeitig und beliebig variieren können, ohne sich gegenseitig zu beeinflussen. Ein Beispiel für ein Einkomponentensystem ist eines mit einer einzigen reinen Chemikalie, während Zweikomponentensysteme, wie Mischungen aus Wasser und Ethanol, zwei unabhängige Komponenten haben. Typische Phasenübergänge (Phasengleichgewicht) sind Festkörper, Flüssigkeiten, Gase.
Phasenregel bei konstantem Druck
Für Anwendungen in den Materialwissenschaften, die sich mit Phasenänderungen zwischen verschiedenen festen Strukturen befassen, tritt häufig ein konstanter Druck auf (z. B. eine Atmosphäre) und wird als Freiheitsgrad ignoriert, sodass die Regel lautet: F=C - P + 1.
Diese Formel wird manchmal unter dem Namen "Kondensierte-Phasen-Regel" eingeführt, ist aber bekanntermaßen nicht auf diese Systeme anwendbar, die hohen Drücken ausgesetzt sind (z. B. in der Geologie), da dies Folgen hat Druck kann katastrophale Folgen haben.
Es mag den Anschein haben, dass das Phasengleichgewicht nur eine leere Phrase ist und es nur wenige physikalische Prozesse gibt, in denen dieser Moment stattfindetist beteiligt, aber wie wir gesehen haben, funktionieren viele der Gesetze, die wir kennen, ohne sie nicht, also müssen Sie sich ein wenig mit diesen einzigartigen, farbenfrohen, wenn auch etwas langweiligen Regeln vertraut machen. Dieses Wissen hat vielen Menschen geholfen. Sie haben gelernt, sie auf sich selbst anzuwenden, zum Beispiel können Elektriker, die die Regeln für die Arbeit mit Phasen kennen, sich vor unnötigen Gefahren schützen.

