Gase werden aus thermodynamischer Sicht durch eine Reihe makroskopischer Eigenschaften beschrieben, deren wichtigste Temperatur, Druck und Volumen sind. Die Konstanz eines dieser Parameter und die Änderung der anderen beiden zeigt an, dass der eine oder andere Isoprozess im Gas auftritt. Wir werden diesen Artikel einer detaillierten Antwort auf die Fragen widmen, dass dies ein isochorer Prozess ist, wie er sich von isothermen und isobaren Änderungen in den Zuständen eines Gassystems unterscheidet.
Ideales Gas in der Physik

Bevor du die Frage beantwortest, dass es sich um einen isochoren Prozess handelt, solltest du dich mit dem Konzept eines idealen Gases vertraut machen. In der Physik versteht man darunter jedes Gas, in dem die durchschnittliche kinetische Energie seiner Teilchen die potentielle Energie ihrer Wechselwirkung weit übersteigt und die Abstände zwischen diesen Teilchen um mehrere Größenordnungen größer sind als ihre linearen Abmessungen. Unter den angegebenen Bedingungen ist es möglich, bei der DurchführungBerechnungen berücksichtigen nicht die Wechselwirkungsenergie zwischen Teilchen (sie ist gleich Null), und es kann auch angenommen werden, dass die Teilchen materielle Punkte mit einer bestimmten Masse m sind.
Der einzige Prozess, der in einem idealen Gas stattfindet, ist der Zusammenstoß von Teilchen mit den Wänden des Gefäßes, das die Substanz enthält. Diese Stöße äußern sich in der Praxis durch das Vorhandensein eines bestimmten Drucks im Gas P.
In der Regel kann jeder gasförmige Stoff, der aus chemisch relativ inerten Molekülen besteht und einen niedrigen Druck und eine hohe Temperatur aufweist, als ideales Gas mit ausreichender Genauigkeit für praktische Berechnungen angesehen werden.
Gleichung, die ein ideales Gas beschreibt
Natürlich sprechen wir über das universelle Gesetz von Clapeyron-Mendeleev, das gut verstanden werden sollte, um zu verstehen, dass dies ein isochorischer Prozess ist. Die universelle Zustandsgleichung hat also folgende Form:
PV=nRT.
Das heißt, das Produkt aus dem Druck P und dem Gasvolumen V ist gleich dem Produkt aus der absoluten Temperatur T und der Stoffmenge in Mol n, wobei R der Proportionalitätsfaktor ist. Die Gleichung selbst wurde erstmals 1834 von Emile Clapeyron niedergeschrieben, und in den 70er Jahren des 19. Jahrhunderts ersetzte D. Mendeleev darin einen Satz konstanter Werte einer einzigen universellen Gaskonstante R (8,314 J/(molK)).
Nach der Clapeyron-Mendeleev-Gleichung bleibt in einem geschlossenen System die Anzahl der Gasteilchen konstant, sodass sich nur drei makroskopische Parameter ändern können (T, Pund V). Die letztere Tatsache liegt dem Verständnis der verschiedenen Isoprozesse zugrunde, die weiter unten diskutiert werden.
Was ist ein isochorer Prozess?
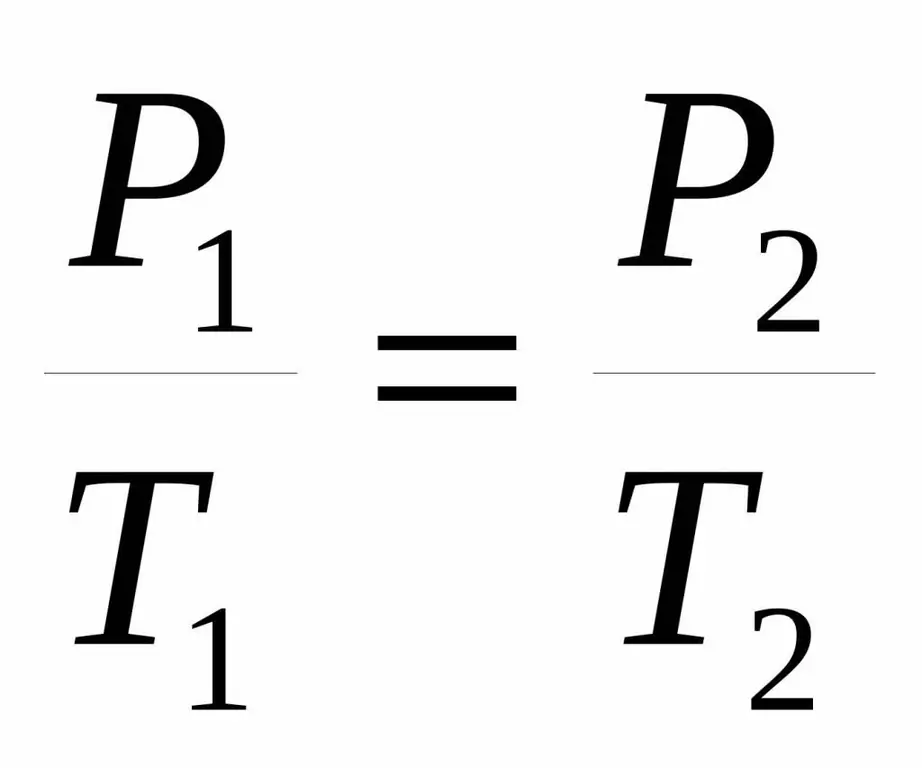
Unter diesem Vorgang versteht man absolut jede Zustandsänderung des Systems, bei der dessen Volumen erh alten bleibt.
Wenn wir uns der universellen Zustandsgleichung zuwenden, können wir sagen, dass sich bei einem isochoren Prozess in einem Gas nur der Druck und die absolute Temperatur ändern. Um genau zu verstehen, wie sich die thermodynamischen Parameter ändern, schreiben wir den entsprechenden mathematischen Ausdruck:
P / T=konst.
Manchmal wird diese Gleichheit in einer etwas anderen Form angegeben:
P1 / T1=P2 / T 2.
Beide Gleichungen heißen Karlsgesetz nach dem Namen eines französischen Wissenschaftlers, der Ende des 18. Jahrhunderts die erwähnte Abhängigkeit experimentell ermittelte.

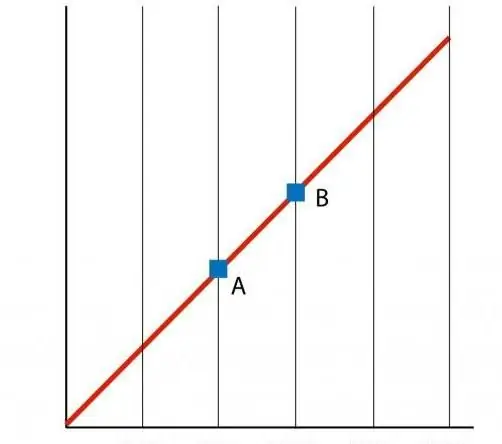
Wenn wir einen Graphen der Funktion P(T) erstellen, erh alten wir eine geradlinige Abhängigkeit, die Isochore genannt wird. Jede Isochore (für alle Werte von n und V) ist eine Gerade.
Energiebeschreibung des Prozesses
Wie bereits erwähnt, ist ein isochorer Prozess eine Zustandsänderung eines Systems, die in einem geschlossenen, aber nicht isolierten System stattfindet. Wir sprechen von der Möglichkeit des Wärmeaustauschs zwischen dem Gas und der Umgebung. Im Allgemeinen führt jede Zufuhr von Wärme Q zum System zu zwei Ergebnissen:
- ändert die innere Energie U;
- Gasfunktioniert A, expandierend oder kontrahierend.
Der letzte Schluss wird mathematisch wie folgt geschrieben:
Q=U + A.
Der isochore Prozess eines idealen Gases impliziert per Definition keine vom Gas verrichtete Arbeit, da sein Volumen unverändert bleibt. Dies bedeutet, dass die gesamte dem System zugeführte Wärme dazu dient, seine innere Energie zu erhöhen:
Q=U.
Wenn wir die explizite Formel für innere Energie in diesen Ausdruck einsetzen, dann kann die Wärme des isochoren Prozesses dargestellt werden als:
Q=z / 2nRT.
Hier ist z die Anzahl der Freiheitsgrade, die durch die mehratomige Natur der Moleküle bestimmt wird, aus denen das Gas besteht. Für ein einatomiges Gas ist z=3, für ein zweiatomiges Gas - 5 und für ein dreiatomiges und mehr - 6. Unter den Freiheitsgraden verstehen wir hier Translations- und Rotationsgrade.
Wenn wir die Effizienz der Erwärmung eines Gassystems in isochoren und isobaren Prozessen vergleichen, erh alten wir im ersten Fall die maximale Effizienz, da sich das Gas während der isobaren Zustandsänderung des Systems ausdehnt und ein Teil der zugeführten Wärme wird für die Arbeit aufgewendet.
Isobarer Prozess
Oben haben wir ausführlich beschrieben, dass es sich um einen isochoren Prozess handelt. Lassen Sie uns nun ein paar Worte über andere Isoprozesse sagen. Beginnen wir mit Isobaren. Aufgrund des Namens versteht man darunter den Übergang des Systems zwischen Zuständen bei konstantem Druck. Dieser Vorgang wird durch das Gay-Lussac-Gesetz wie folgt beschrieben:
V / T=konst.
Wie bei der Isochore stellt auch die V(T)-Isobare eine gerade Linie in der Grafik dar.
FürBei jedem isobaren Prozess ist es bequem, die vom Gas verrichtete Arbeit zu berechnen, da sie gleich dem Produkt aus konstantem Druck und Volumenänderung ist.
Isothermischer Prozess
Dies ist ein Vorgang, bei dem die Temperatur des Systems konstant bleibt. Es wird durch das Boyle-Mariotte-Gesetz für ein ideales Gas beschrieben. Es ist merkwürdig festzustellen, dass dies das erste experimentell entdeckte Gasgesetz ist (zweite Hälfte des 17. Jahrhunderts). Seine mathematische Schreibweise sieht so aus:
PV=const.
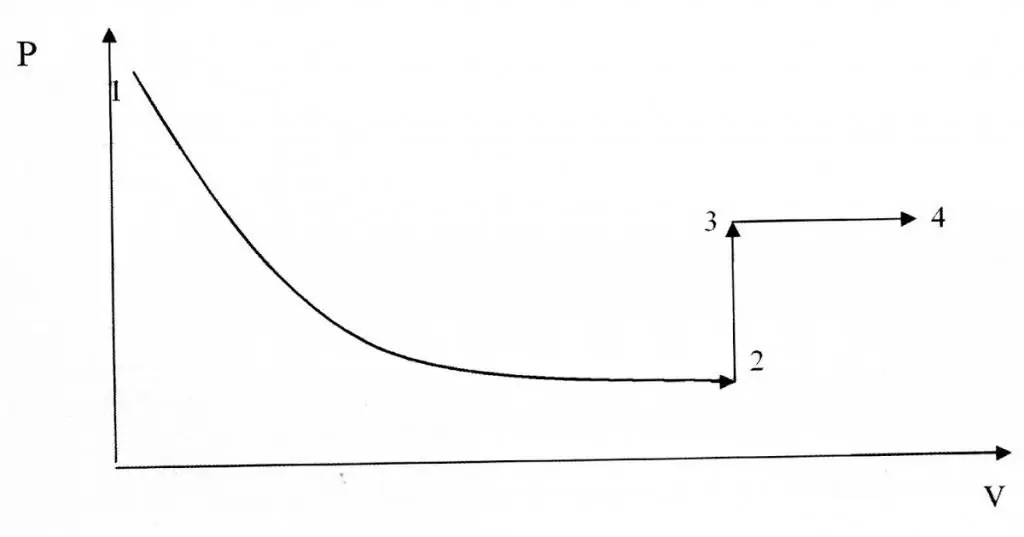
Isochore und isotherme Prozesse unterscheiden sich in ihrer grafischen Darstellung, da die Funktion P(V) ein hyperbolischer, kein linearer Zusammenhang ist.
Beispiel zur Problemlösung
Konsolidieren wir die theoretischen Informationen aus dem Artikel durch ihre Anwendung zur Lösung eines praktischen Problems. Es ist bekannt, dass sich reiner gasförmiger Stickstoff in einer Flasche bei einem Druck von 1 Atmosphäre und einer Temperatur von 25 °C befand. Nachdem die Gasflasche erhitzt und der Druck darin gemessen wurde, stellte sich heraus, dass er 1,5 Atmosphären betrug. Welche Temperatur hat das Gas in der Flasche nach dem Aufheizen? Um welchen Betrag ändert sich die innere Energie des Gases, wenn sich 4 Mol Stickstoff im Ballon befinden.
Um die erste Frage zu beantworten, verwenden wir den folgenden Ausdruck:
P1 / T1=P2 / T 2.
Woher wir bekommen:
T2=P2 / P1 T 1.
In diesem Ausdruck kann der Druck durch beliebige Einheiten ersetzt werdenMessungen, da sie schrumpfen und die Temperatur nur in Kelvin angezeigt wird. Damit erh alten wir:
T2=1,5 /1298,15=447,224 K.
Die berechnete Temperatur in Grad Celsius beträgt 174 °C.
Da das Stickstoffmolekül zweiatomig ist, kann die Änderung seiner inneren Energie beim Erhitzen wie folgt bestimmt werden:
ΔU=5 / 2nRΔT.
Indem wir die bekannten Werte in diesen Ausdruck einsetzen, erh alten wir die Antwort auf die zweite Frage des Problems: ΔU=+12,4 kJ.






